HNO3 Nedir, Asit Mi Baz Mı, Nerelerde Kullanılır? HNO3 Yaygın Adı, Kullanım Alanları ve pH Değeri Nedir?
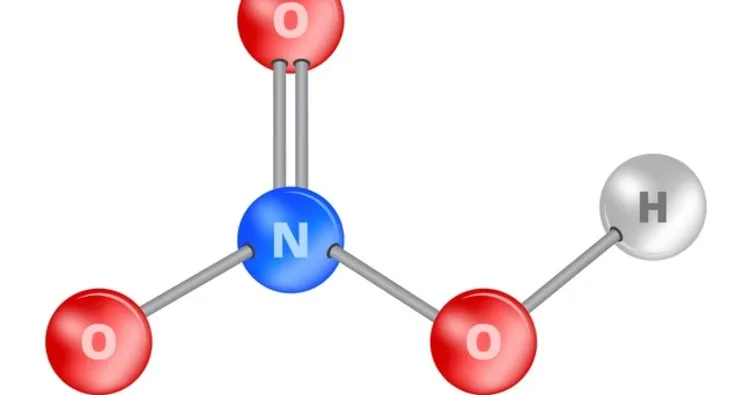
HNO3 maddesinin kimyasal adı nitrik asittir. İçinde bir hidrojen (H), bir azot (N) ve 3 oksijen (O) atomu bulundurur. Halk arasında kezzap olarak bilinir. HNO3 maddesinin farklı yoğunluklardaki çözeltilerine farklı isimler verilir ve rengi de belirli yoğunluklarda farklılık gösterebilmektedir.
İlk olarak Uzak Doğu ve Antik Yunan'da 1200lü yıllarda bulunan nitrik asit simyada sıkça kullanılmıştır. Günümüzde ise temizlik maddelerinden patlayıcı yapımına kadar birçok farklı alanda kullanılıyor. Zehirli bir duman olan nitrik asit insan dokularını tahriş edici özelliğe sahip olmakla birlikte alt solunum yollarına da etki eder. Bu özellikleriyle HNO3 nerede kullanılır sorusu akılları kurcalamaktadır.
HNO3 NEDİR?
HNO3 bileşiğinin adı nitrik asittir ve halk arasında kezzap olarak bilinir. Güçlü, aşındırıcı, inorganik bir asittir. Birçok metali çözebilir. HNO3 molekül ağırlığı 63.02 g/mol dür.
HNO3, yoğunluğuna göre farklı isimler alabilir:
- Saf nitrik asit: Mutlak nitrik asit olarak bilinir. Renksiz bir yapıdadır.
- %95'den yoğun nitrik asit çözeltileri: Beyaz dumanlı nitrik asit
- %86'dan yoğun nitrik asit çözeltileri: Kırmızı dumanlı nitrik asit
- %68'den yoğun nitrik asit çözeltileri: Ticari olarak satışı yapılan nitrik asit türüdür. Halk arasında kezzap olarak bilinen nitrik asit türüdür.
Geçmiş dönemlerde nitrik asit üretimi güherçile yardımıyla yapılırdı fakat bu ürünün bulunması hayli zordur. Bu sebeple ünümüzde farklı üretim şekillerinin doğmuştur. Amonyak endüstrisinin gelişmiş olduğu ülkelerde nitrik asit üretiminde amonyak kullanılır. Katalizör yardımıyla gaz halindeyken havada azot döngüsü yaratılarak amonyak üretilir. Buna Ostwald metodu adı verilmektedir. Bu metot ile uygun hava akımı elektrik arkı ile yaratılmış yüksek sıcaklıktan geçirilir. Bu esnada azot ve oksijen birleşerek azot oksit oluşur. Soğuk hava akımında yeniden oksijen ve suyla birleştirildiğinde ise nitrik asit oluşur.
Nitrik asit genellikle başka maddelerin üretiminde hammadde olarak kullanılır. HNO3 kullanım alanları ise başlıca gübre üretimi, patlayıcı madde üretimi, pH dengeleme, su arıtımı, metal imalatı ve boya sanayiidir.
HNO3 ASİT Mİ BAZ MI?
HNO3 bir hidrojen (H), bir azot (N) ve 3 oksijen (O) atomlarından oluşur. Bir mol HNO3'ün sulu ortamda ayrışması ile H+ atomu verir. Sulu çözeltilerinde H atomu veren bileşikler asittir yani HNO3 asittir.
Sıvıların pH değeri çözeltilerin asitlik bazlık derecelerini gösterir ve turnusol kağıdı, gösterge çubukları, pH metre gibi araçlarla ölçülür. pH değeri 7 olan maddeler nötrdür. 7'den büyük pH değerine sahip maddeler baz, düşük olanlar asit olarak ifade edilir. HNO3 pH değeri 1'dir.








